活性污泥法是以活性污泥为核心的废水生物处理技术,其中对污染物降解起关键作用的是活性污泥中的细菌[1],而作为细菌的捕食者——微型动物在维持细菌群落活力[2],为活性污泥中的细菌提供矿物营养[3],维护活性污泥微环境生态食物链健康[4],维持活性污泥系统稳定[5]发挥重要作用,可作为活性污泥法废水处理效能的指示生物[6~9].
水中存在的有毒有害物质一方面会对活性污泥中的不同类别细菌产生不同程度的抑制效应,对细菌群落结构产生影响,进而通过食物链的传递影响到处于食物链顶端的微型动物的群落结构[10];另一方面,毒害物直接对微型动物产生毒害效应,如重金属离子[11, 12],从而对活性污泥微型动物群落结构产生重要影响.
苯酚是生产某些聚合树脂、造纸、精炼石油以及药物(如阿司匹林)等工业过程生产废水中的主要污染物[13],当进入废水生物处理系统时,会对活性污泥微生物产生影响,从而影响到废水处理效果.目前,苯酚对活性污泥处理系统的毒害研究主要集中于活性污泥处理性能[14, 15]、污泥特性[16]、代谢机制[17]、动力学[18]和细菌群落结构[19]等方面.为了筛选出苯酚对活性污泥处理性能(运行参数、处理效果等)的指示生物而进行了少量的微型动物研究[8, 20],而未从群落结构动态变化的角度揭示苯酚对活性污泥的微生态系统的长期影响机制.
本研究的主要目的是基于序批式活性污泥处理系统(SBR),探究含酚废水对活性污泥活性及微型动物群落结构的持续负荷影响,并探讨污泥活性与微型动物群落之间的关系,筛选污泥活性指标的指示生物,以期为含酚废水生物处理系统的生产运行提供生物学理论及技术依据.
1 材料与方法
1.1 装置启动与运行控制
自制序批式反应器(SBR),其主体由高85 cm、内径7.5 cm的有机玻璃柱制成,有效容积为3.2 L.空气压缩机通过置于反应器底部的微孔曝气头提供系统所需氧气,同时为泥、水的混匀与环流提供动力.通过调节空气流量计控制曝气强度(0.2 L ·min-1),维持水中稳定的溶解氧(DO)[(6.02±0.47) mg ·L-1].反应器在室温[(21.6±4.2)℃]下运行.分别设置对照系统CK(进水不添加苯酚)和试验系统EK[进水添加苯酚(aladdin试剂,分析纯)]这2个系统.
接种污泥取自马鞍山市某污水处理厂好氧池,采用自来水对污泥进行清洗并均混后分别投加至2个反应器,闷曝2 d后,混合液悬浮固体浓度(MLSS)分别为2 753 mg ·L-1和2 669 mg ·L-1,污泥沉降比(SV)均为22%.然后进行污泥培养驯化,培养原水由静置48 h的自来水混合配制而成,水中投加一定量的C6H12O6、 NH4Cl、 KH2PO4(微量元素来源于试验用水),使BOD :N :P之比接近100 :5 :1.用NaHCO3/Na2CO3缓冲体系(pH=9.25)调节进水pH(7.60±0.10).通过系统中活性污泥微型动物群落物种多样性及出水水质等指标判定[11],系统运行约30 d,活性污泥达初步成熟,完成驯化,进行正式试验.
正式试验分成3个阶段,在培养原水中加入不同量高浓度苯酚溶液(50g ·L-1),使第1、第2、第3阶段原水中苯酚溶液浓度分别为50 mg ·L-1(低浓度)、 100 mg ·L-1(中等浓度)和300 mg ·L-1(高浓度);试验期间,系统的进水水质控制在COD为(839.04±87.70) mg ·L-1、氨氮为(45.22±4.95) mg ·L-1、总磷为(6.65±0.34) mg ·L-1,系统中污泥负荷(以COD/MLSS计)约为0.25 kg ·(kg ·d)-1.
正式试验期,反应器采用间歇曝气的方式运行(曝气和沉淀交替进行,时间均为2 h),每天运行2个周期,每个周期12 h.在每个周期沉淀结束前将反应器中上清液通过出水口排出,排水比(进水体积与反应池总有效体积之比)为1/3.2,然后补入新鲜原水至原水位,重新进入下一个周期运行,如此循环往复.通过每日在曝气阶段末期排放一定量泥水混合液的方式控制MLSS在4 000 mg ·L-1左右,并控制污泥龄θ为25 d.
1.2 样品采集及微型动物鉴别计数与分类
正式试验开始后,每隔1~2 d在第1个周期(08:00~20:00)最后一个曝气阶段结束前30 min内,通过虹吸管在反应器垂直方向上等距离(反应器底部往上10、 40、 70 cm处)采集3个污泥混合液平行样用于微型动物鉴别计数.
使用微量移液器(DRAGON大龙)移取25 μL[单独取样鉴别统计小型鞭毛虫(flagellates)(≤20 μL)时取样量为5 μL]摇匀后的污泥混合液置于光学显微镜(PH50系列, ×100或×400)下对微型动物进行鉴别、计数.根据形态学和行为学特征并依照图谱、文献[21, 22]将微型动物按需要鉴定到种或类群.原生动物均鉴定到种,轮虫(rotifers)、线虫(nematodas)等微型后生动物鉴定到类群[23].鉴定工作在5 h(最长不超过8 h)内完成,以避免微型动物数量和物种丰富程度在鉴别过程中改变[23, 24].将微型动物群落中常见的纤毛虫类原生动物分为菌食性纤毛虫(Bacterivorous ciliates)和肉食性纤毛虫(Carnivorous ciliates),其中菌食性纤毛虫又分为匍匐型纤毛虫(Crawling ciliates)、固着型纤毛虫(Sessile ciliates)和游泳型纤毛虫(Swimming ciliates)等三大类群[23],将微型动物数量所得数据折算成个·mL-1.
1.3 污泥活性与水质及污泥常规指标测定
每隔2~3 d在第1个周期最后一个曝气阶段结束前30 min内取一定量的泥水混合液进行污泥电子传递体系(electron transport system, ETS)包括TTC-ETS和INT-ETS活性测定[25, 26].其中,抑制率(IR)计算公式为:
式中,R0为对照系统测定值,R为试验系统测定值.
在进水曝气后的1 min内取少量混匀后的泥水混合液过滤(0.45 μm微滤膜),采用紫外-可见分光光度法(上海仪电752N)测定滤液中实际苯酚浓度(最大吸收波长为270 nm).其他指标:化学需氧量(COD)、氨氮(NH4+-N)、总磷(TP)按照标准方法[27]测定;污泥沉降比(SV)采用30 min沉降直接读数法测定;混合液悬浮固体浓度(MLSS)采用重量法测定;溶解氧(DO)和水温(T)采用便携式溶解氧测定仪(雷磁JPBJ-608)测定;pH值采用数显pH计(雷磁PHS-25)测定.
1.4 数据处理分析
采用Shannon-Wiener指数[28]H′表征活性污泥微型动物群落物种多样性,其计算公式:
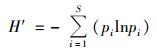
式中,S表示物种种数,pi表示第i个种的个体数占所有物种总数的百分比.
所有微型动物统计数据均取3个平行样平均值进行分析.统计分析采用软件SPSS 19.0进行Pearson相关性、 LSD多重比较(α=0.05)和主成分分析(PCA),其中Pearson相关性分析之前需将所有原始数据按对数公式x=ln(x+1)进行转换.采用Origin 9.0和Excel 2007完成相关图表制作.
2 结果与讨论 2.1 污泥活性对苯酚毒害效应的响应及其变化
在整个试验过程中,两个活性污泥系统的处理效果没有明显的差异(P>0.05)[试验过程中,两个系统COD和NH4+-N去除率分别为(95.38±4.41)%、 (97.06±2.42)%和(98.92±1.58)%、 (98.46±2.29)%],可能的原因是在足够长的反应时间(本试验曝气反应时间为6 h)条件下对一定范围内浓度(<400 mg ·L-1)的进水苯酚能够作为碳源的一部分被细菌充分降解,以致对活性污泥处理效果不产生明显影响[14, 16].但进水浓度在400 mg ·L-1以下的苯酚对好氧污泥形态、比耗氧速率(SOUR)[16]以及活性污泥微型动物群落种属组成[20]均有明显的影响.
电子传递体系(ETS)活性可表征活性污泥系统中的微生物活性[26, 29~31],揭示系统硝化反硝化规律[26],表征重金属对污泥活性的影响[32, 33]. TTC-ETS和INT-ETS是用于检测污泥ETS活性的常用方法[34],两者因氧化还原电位大小以及从呼吸链上接受电子的部位不同(后者较早地从呼吸链上接受电子)而对污泥活性的响应不同[25, 35].然而,是否可以采用污泥ETS活性表征酚类有机毒害物质对污泥活性的影响,未见报道.本研究通过测定TTC-ETS活性和INT-ETS活性,分析比较确定适用于有机毒害物苯酚对污泥活性影响的有效表征指标,以揭示在苯酚毒害效应影响下污泥活性的变化规律.不同进水苯酚浓度持续负荷条件下污泥TTC-ETS活性、 INT-ETS活性及其动态变化如表 1和图 1所示.
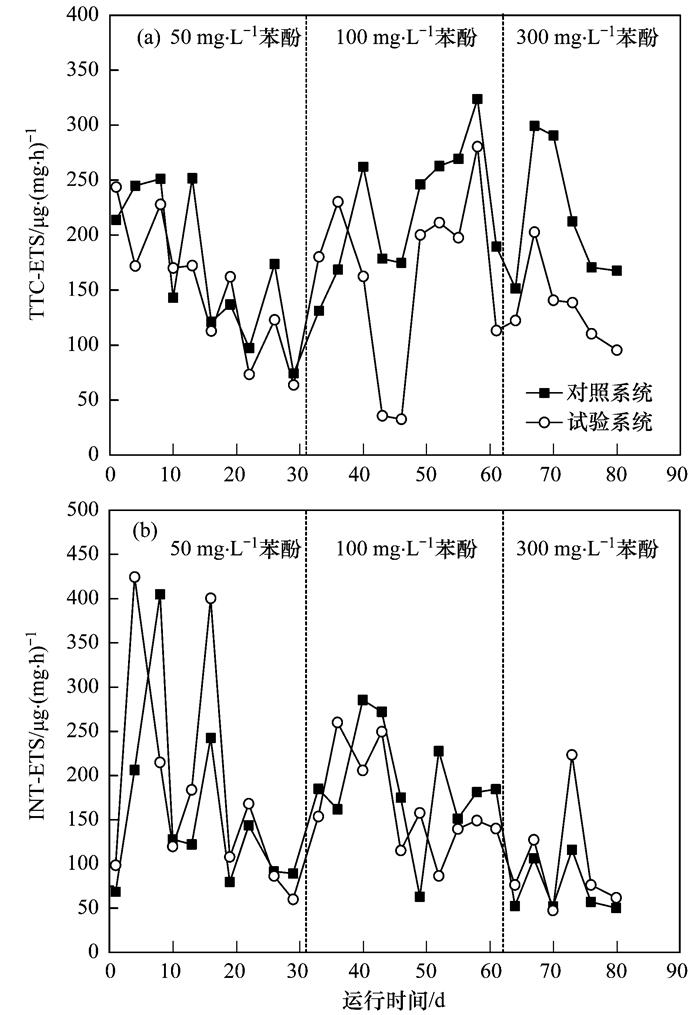
图 1 苯酚对活性污泥TTC-ETS活性和INT-ETS活性的影响

表 1 不同进水苯酚浓度持续负荷条件下污泥ETS活性1)
从图 1(a)中可以看出,在整个试验期间内,对照系统CK、试验系统EK中的污泥TTC-ETS活性分别为(200.26±65.57) μg ·(mg ·h)-1、 (152.91±63.63)μg ·(mg ·h)-1,均存在较大波动,且变化趋势相近,这与前人的研究结论[31]相一致,即进水水质等运行参数的改变不会影响SBR系统中污泥TTC-ETS活性的变化趋势.当进水苯酚为低浓度(50 mg ·L-1)时,苯酚的毒害效应对系统中污泥TTC-ETS活性的影响并不显著(P=0.499),其抑制率IR仅为(20.75±10.43)%(图 2,下同);当进水苯酚浓度增加到100 mg ·L-1时,CK、 EK两个系统中TTC-ETS活性均随运行时间变化而有所增大,且EK系统的TTC-ETS活性此阶段的初期更大,试验第36 d为230.30 μg ·(mg ·h)-1,比CK系统[168.57 μg ·(mg ·h)-1]大36.62%,这说明适当浓度的苯酚会短暂地促进污泥TTC-ETS活性的增大. ETS活性表征污泥活性的方法实质上是通过测定好氧微生物的呼吸活性来间接指示活性污泥的生物活性[34],故适当浓度的苯酚短时间内能够通过促进TTC-ETS活性的增长(活性污泥中微生物的呼吸增强)来增强微生物(包括微型动物,下同)对苯酚毒性生存环境的适应.随后TTC-ETS活性开始降低,系统运行第46 d,试验系统中污泥TTC-ETS活性达到最低的32.61 μg ·(mg ·h)-1,仅有对照系统的18.66%,抑制率高达81.34%.这是因为随着时间的推移,苯酚在活性污泥中得到累积,超过污泥中微生物的耐受阈值,微生物开始大量死亡,导致污泥活性急剧降低,污泥TTC-ETS活性呈现出急剧减小的趋势.第50 d,两个系统中的污泥TTC-ETS活性逐步增大,且两者的差距逐渐缩小,这是由于试验系统中的活性污泥某些微生物通过驯化,逐步适应了有毒的生存环境,大量繁殖的结果.总的看来,进水苯酚浓度为100 mg ·L-1时,试验系统与对照系统中污泥TTC-ETS活性存在显著差异(P=0.045)(表 1,下同),说明此浓度下的苯酚毒性对污泥活性产生了明显的抑制效应;进一步增大进水苯酚浓度至300 mg ·L-1,试验系统与对照系统中的污泥TTC-ETS活性差异性进一步增大(P=0.008),但在这一阶段后期,苯酚对污泥TTC-ETS活性的抑制率相对稳定在40%左右.
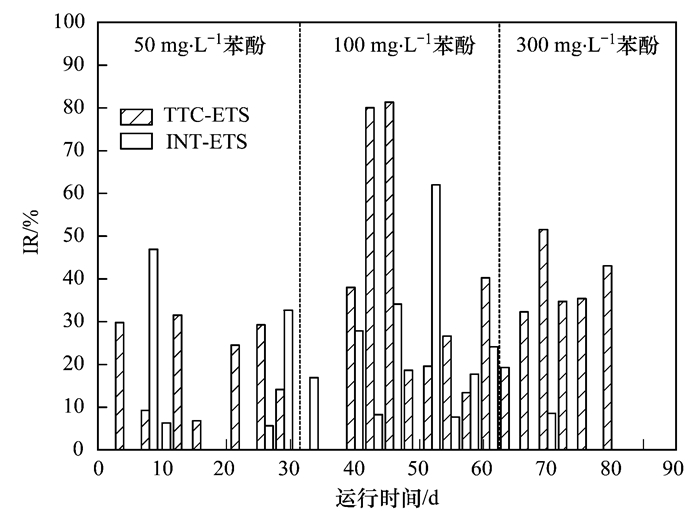
不包括0~100%以外的数据 图 2 苯酚对活性污泥TTC-ETS活性、INT-ETS活性的抑制影响
图 1(b)表明:在整个试验过程中试验系统和对照系统具有相近的INT-ETS活性变化规律,这与TTC-ETS活性类似.然而,LSD多重比较分析结果表明(表 1),进水苯酚浓度在50~300 mg ·L-1范围内,苯酚对污泥INT-ETS活性几乎没有显著影响(P>0.05),这可能是因为INT较早地从呼吸链上接受电子,只有细胞色素b之前的电子传递过程被阻断后其活性才能受到抑制,因此INT-ETS活性受影响的概率要小一些[25].此外,TTC氧化还原电位(460 mV)明显高于INT氧化还原电位(90 mV)[35],TTC作为人工电子受体时在进水浓度在50~300 mg ·L-1范围内的苯酚毒害作用下更容易接受电子发生电化学反应,故污泥TTC-ETS活性比INT-ETS活性更加敏感,更适合作为苯酚对好氧污泥活性毒害效应的响应指标,以反映苯酚对好氧污泥活性的影响规律.
2.2 苯酚对活性污泥微型动物群落结构的影响
2.2.1 苯酚对活性污泥微型动物形态的影响
在试验过程中发现,随着苯酚浓度的增大,试验活性污泥系统中开始出现体型与微型动物大小相近的胞囊(其个体大小为100~300 μm),如虫体收缩状态下的轮虫[图 3(a)],其数量变化规律如图 3(b)所示.由图 3(b)可知,在低浓度条件下,未观察到胞囊,当进水苯酚浓度增大至100 mg ·L-1时,一些微型动物(由观察到的胞囊大小可以判断出并非所有微型动物都形成胞囊)为了避免苯酚毒性环境的毒害,纤毛等消失,身体向内收缩成椭圆形,并在体外积累一层保护膜形成胞囊,这一现象在韦贞鸽等[36]的相关研究中也观察到了.此时,胞囊开始大量出现,第37 d达最大值(4 640个·mL-1).随后开始急剧减少,到第二阶段结束时减至173个·mL-1,在高浓度(300 mg ·L-1)条件下,胞囊数量仍较少,试验结束时,几乎观察不到胞囊,说明过高浓度(>300 mg ·L-1)的苯酚其毒害作用使微型动物形成胞囊的生存机制失效,大量死亡而消失.胞囊是微型动物对毒性的形态适应方式,是一种自我保护的生存机制,也是影响微型动物群落结构动态变化的原因之一,但由于胞囊只是微型动物的休眠体,以下对活性污泥微型动物群落结构进行分析时,不包括胞囊.
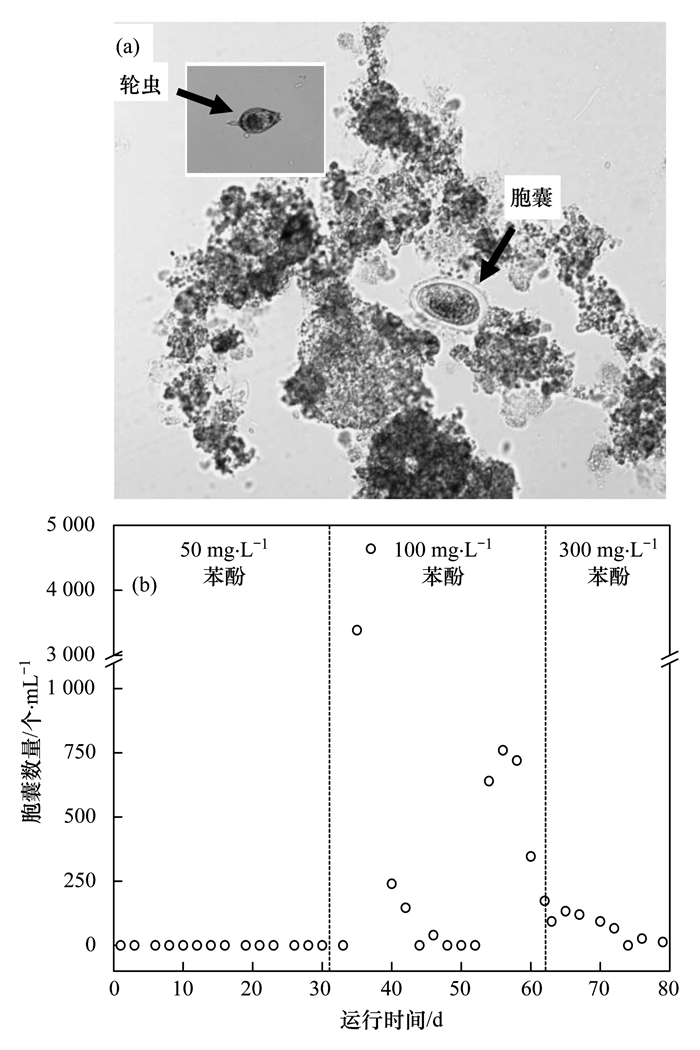
图 3 苯酚毒害作用下微型动物形成的胞囊(100倍)及其数量变化规律
2.2.2 苯酚对活性污泥微型动物群落结构的影响
不同浓度苯酚毒害作用下,活性污泥微型动物群落结构如表 2所示.

表 2 活性污泥系统中微型动物群落不同类群的多度和相对多度1)
从表 2中可知,两个系统中微型动物群落类群组成均在不同运行阶段而所有不同.当进水苯酚浓度为50 mg ·L-1时,除有壳变形虫(P=0.026)外,两个活性污泥系统中的微型动物群落不同类群多度[单位体积(mL)泥水混合液中微型动物个体总数]均不存在显著性差异(P>0.05),整个群落多度也不存在显著性差异(P=0.904),且所有微型动物类群相对多度均不存在显著性差异(P>0.05),说明低浓度苯酚对活性污泥微型动物群落结构没有显著性影响;当进水苯酚浓度增加至100 mg ·L-1时,苯酚对微型动物群落中的固着型纤毛虫(P=0.041)、有壳变形虫(P=0.000)、微型后生动物(P=0.025)等类群以及整个微型动物群落多度(P=0.018)均产生显著性影响,其中裸变形虫和鞭毛虫的相对多度(物种个体数占所有物种总数的百分比)与对照系统相比存在显著性差异(P < 0.05),说明当进水浓度为100 mg ·L-1时,苯酚会对活性污泥微型动物群落结构产生明显的影响;进一步增大进水苯酚浓度至300 mg ·L-1,与对照系统相比,试验活性污泥系统中的匍匐型纤毛虫(P=0.04)、肉食性纤毛虫(P=0.022)、鞭毛虫(P=0.004)也存在显著性差异(P < 0.05),且整个微型动物群落多度差异进一步增大(P=0.014),说明高浓度苯酚长期作用下对活性污泥微型动物群落不同类群产生不同影响:一方面,高浓度苯酚对微型动物群落中的多数类群的生长繁殖存在明显的抑制作用,如匍匐型纤毛虫、肉食性纤毛虫、有壳变形虫、裸变形虫等.另一方面,高浓度苯酚对微型动物群落中的某些类群的生长繁殖也存在明显的促进作用,如鞭毛虫.试验系统鞭毛虫多度[(7 850±4 198)个·mL-1]显著大于对照系统[(2 550±1 089)个·mL-1](表 2),其相对多度达(70.72±20.77)%,成为优势类群.可能的原因是:①在较高浓度苯酚长期作用下,苯酚在活性污泥中累积(水中实际浓度达80~100 mg ·L-1),细菌活力受到抑制,其凝聚能力降低,污泥絮体粒径变小[16],不利于爬行或附着于污泥絮体表面捕食细菌的匍匐型和固着型纤毛虫[37]生长繁殖,而有利于游离于絮体表面活动的鞭毛虫存活,从而使其在微环境食物链中对细菌的捕食更有竞争力而快速繁殖;②相对于体型较大的纤毛虫原生动物,鞭毛虫[尤其是异养型鞭毛虫(HNAN)]对游离细菌的捕食效率更高[38],因而生长繁殖旺盛.此外,高浓度苯酚对微型后生动物中线虫的生长繁殖也有促进作用.更重要的是,与对照系统相比,试验系统中的匍匐型纤毛虫(P=0.038)、肉食性纤毛虫(P=0.016)、有壳变形虫(P=0.040)、鞭毛虫(P=0.001)的相对多度均存在显著性差异(表 2),说明高浓度苯酚的进入会对活性污泥微型动物群落结构产生更为显著的影响.
有研究者认为不同种类在群落中的数量分布曲线是表现群落结构的一个重要指标[21],故在此基础上获得的Shannon-Wiener指数H′可以反映群落结构差异.为了进一步揭示苯酚浓度大小对活性污泥微型动物群落结构的影响程度,对不同浓度条件下微型动物群落物种多样性指数进行主成分分析,结果如图 4所示.从中可知,选取的2个主成分贡献率分别为52.08%、 19.69%,累积贡献率达71.77%.低浓度苯酚持续负荷作用下的活性污泥微型动物群落物种多样性及相应对照系统与PC1和PC2均呈正相关,中等浓度苯酚持续负荷作用下的活性污泥微型动物群落物种多样性与PC1和PC2均呈正相关,而其相应对照系统中的微型动物群落物种多样性与PC2呈负相关,即两者差异明显,说明中等浓度苯酚进水较之低浓度苯酚进水对活性污泥微型动物群落结构影响更大.进一步分析,除对照系统高浓度苯酚持续负荷作用下的微型动物群落物种多样性指数与PC1呈负相关外,其余条件下的微型动物群落物种多样性均与PC1呈正相关,说明高浓度苯酚长期作用下,活性污泥系统中的微型动物群落物种多样性发生了更为明显的变化,即群落结构受到了明显影响.样方之间距离大小反映了方间特征量的相似程度,且距离越近相似程度越高[39].从样方距离来看,低浓度苯酚和中等浓度苯酚对活性污泥微型动物群落物种多样性的影响相接近,而高浓度苯酚作用下的微型动物群落与对照系统相比距离最大,说明高浓度苯酚对微型动物群落物种多样性影响最大,即高浓度苯酚对活性污泥微型动物群落结构影响最大,这与前文分析结果相一致.
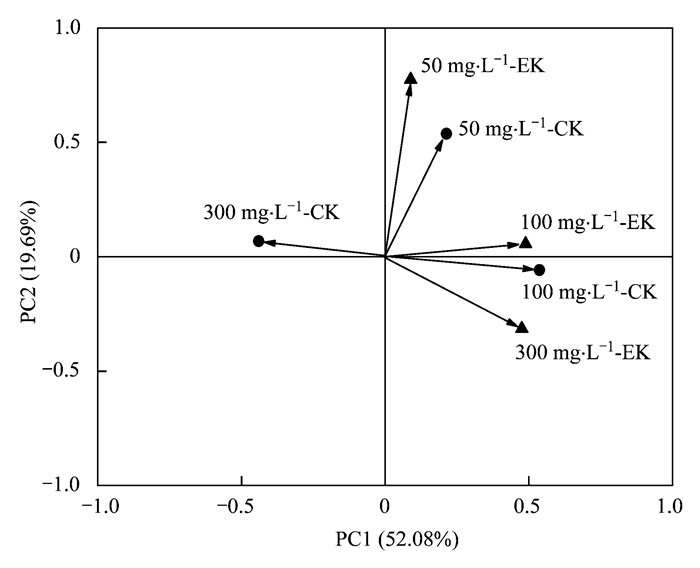
图 4 不同浓度苯酚影响下活性污泥系统中微型动物群落物种多样性主成分分析(PCA)
2.2.3 苯酚影响下活性污泥微型动物群落结构动态变化
活性污泥系统中不同类群微型动物相对多度随运行时间的动态变化如图 5所示.两个系统中不同类群的微型动物其相对多度随运行时间均有较大变化,这与城市废水活性污泥处理系统相一致[37, 40].但不同浓度的苯酚影响下,微型动物群落结构随时间的变化有所不同.具体地,在第1阶段低浓度苯酚进水条件下,除有壳变形虫外,苯酚对微型动物群落不同类群相对多度随时间变化的影响不明显,两个系统中鞭毛虫多度均占据了长时间的绝对优势,其相对多度分别达(64.84±27.56)%、 (75.05±28.18)%,两者无显著性差异(P=0.342),其他类群相对多度较小,且各类群的微型动物相对多度随时间变化趋势线上的拐点所在时间轴的位置相对差异较小(图 5);试验第2阶段,两个系统中各微型动物类群分布相对第1阶段较均匀,在这一阶段有壳变形虫成为优势类群,但试验系统中有壳变形虫前期(32~45d)受到了抑制,对照系统和试验系统中有壳变形虫相对多度分别为(34.31±7.66)%、 (25.66±18.18)%,后者波动也较大.在这一阶段,苯酚对固着型纤毛虫也产生了明显的抑制,其相对多度处于较低水平[(9.58±9.61)%],而鞭毛虫相对多度[(33.76±13.80)%]显著大于后者[(20.53±9.81)%](P=0.005);试验第3阶段,对照系统中微型动物群落各类群分布较均匀,而试验系统中鞭毛虫占绝对优势,试验结束前其相对多度达最大值的91.13%.此外,与对照系统相比,试验系统中的匍匐型纤毛虫和肉食性纤毛虫受到了明显的抑制,前者运行70 d几乎消失,而后者相对多度一直处于极低水平[(1.01±1.05)%].
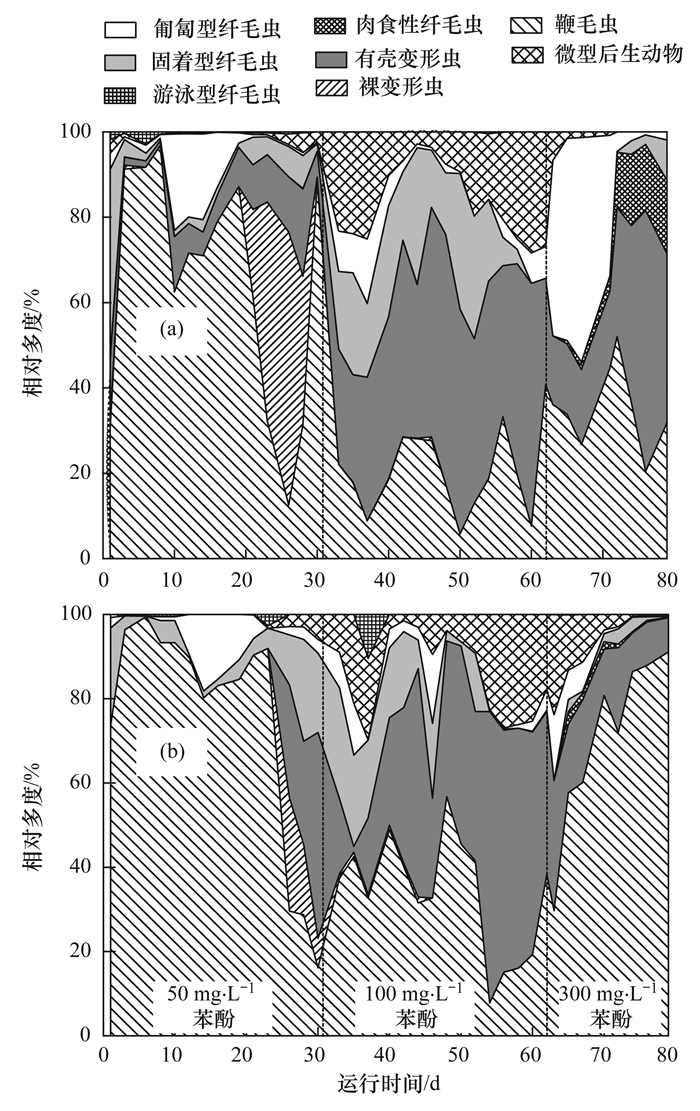
(a)对照系统,(b)试验系统 图 5 两个活性污泥系统中微型动物群落结构动态变化
2.3 苯酚影响下的污泥活性与微型动物间的相互关系探讨
如前文所述,污泥TTC-ETS活性比INT-ETS活性更加敏感,更适合作为苯酚对好氧污泥活性毒害作用的响应指标,故选择TTC-ETS活性作为苯酚影响下污泥活性的表征指标.不同进水浓度苯酚作用下污泥TTC-ETS活性的变化规律[图 1(a)]与活性污泥微型动物群落结构动态变化(图 5)对比分析可知,污泥TTC-ETS活性与微型动物群落结构相互之间存在着一定的关联,如低浓度苯酚对污泥TTC-ETS活性及微型动物群落结构的影响均不明显;当进水浓度达100 mg ·L-1时,苯酚对污泥TTC-ETS活性及微型动物群落结构产生明显的影响;进一步增大进水浓度时,这种影响显著增大.活性污泥是活性污泥处理系统中的主体,而活性污泥微生物是活性污泥污染物降解核心,因此活性污泥微生物ETS活性对活性污泥处理系统的正常运行有着重要意义[41],而在活性污泥微环境生态系统中微型动物作为食物链顶端的捕食者,在维持活性污泥微环境生态系统的稳定发挥着重要作用,因此,活性污泥活性与微型动物群落结构之间也必然存在联系.活性污泥微型动物与污泥活性Pearson相关性分析结果如表 3所示.


表 3 活性污泥微型动物与污泥活性Pearson相关性
水中毒害物质的存在使微型动物群落与所处的微生态环境之间的关系复杂化[42],两个活性污泥系统中的微型动物同一个种与对应污泥活性之间的相关性不同(表 3).为了使所筛选的指示生物对含酚废水活性污泥处理工艺的操作运行具有实际指导意义,选择含苯酚进水系统(即试验系统)作为分析对象,以筛选出含酚废水活性污泥法处理过程中对污泥TTC-ETS活性具有指示价值的微型动物种.在试验过程观察到的活性污泥微型动物群落物种中与污泥活性显著相关的种只有针棘匣壳虫(Centropyxis aculeata,r=-0.628, P < 0.05),说明针棘匣壳虫的大量繁殖,预示着处理含酚废水的污泥活性低.此外,其他微型动物种如湖累枝虫(Epistylis lacustris,r=0.371, P=0.173)、多变斜板虫(Plagiocampa mutabilis,r=-0.403, P=0.137)、软波豆虫(Bodo lens,r=0.418, P=0.121)、跳侧滴虫(Pleuromonas jaculans, r=0.438, P=0.102)等与污泥活性也存在明显的相关性(|r|为0.3~0.5),也可作为含酚废水处理过程中污泥活性的指示生物.
以前的研究都是通过筛选与废水处理指标紧密相关的微型动物种作为活性污泥处理性能某些指标的指示生物[9, 43~45],而本研究说明某些微型动物种与污泥ETS活性之间存在着明显的相关性,即也可作为活性污泥废水处理过程中ETS活性的指示生物.
3 结论
(1) 比较分析TTC-ETS活性及INT-ETS活性等两个ETS活性指标结果表明,污泥TTC-ETS活性能够更有效表征苯酚对污泥活性的影响,且随着进水苯酚浓度的增大,苯酚对污泥活性的抑制越明显,如50 mg ·L-1进水条件下,苯酚对污泥活性的抑制率为(20.75±10.43)%,而300 mg ·L-1进水运行后期,其抑制率稳定在40%左右.
(2) 苯酚对活性污泥微型动物群落结构的影响随浓度的增大而增大,且对不同微型动物类群影响不同.在50 mg ·L-1进水条件下,苯酚只对有壳变形虫存在明显的抑制作用,而进水浓度增大至100 mg ·L-1时,苯酚对固着型纤毛虫、有壳变形虫、微型后生动物等类群以及整个微型动物群落均产生显著性影响.当进水浓度为300 mg ·L-1时,苯酚对匍匐型纤毛虫、肉食性纤毛虫的生长繁殖均有明显的抑制作用,而对鞭毛虫的生长却存在明显的促进作用.
(3) 苯酚对活性污泥微型动物群落结构的动态变化有影响,且进水浓度不同对微型动物群落结构动态随时间变化的影响程度不同.随着苯酚浓度的增大,某些微型动物会形成胞囊自我保护,这种自我保护的生存机制可能是影响微型动物群落结构动态变化的原因之一,但进水苯酚浓度过高(>300 mg ·L-1)时,会导致这种生存机制逐渐失效.
(4) 苯酚影响下的污泥活性与微型动物之间存在某种程度的关联,某些微型动物种可作为污泥活性大小的指示生物,如针棘匣壳虫(Centropyxis aculeata)的大量繁殖,预示着处理含酚废水的污泥活性低;湖累枝虫(Epistylis lacustris)多度与污泥活性呈明显的正相关关系(r=0.371, P=0.173),可作为污泥活性高的指示生物等.(来源及作者:安徽工业大学建筑工程学院 胡小兵、饶强、唐素兰、姜晶、谢瑞桃、郝文静、钟梅英)



