铜广泛应用于电镀、印染以及电池制造等行业.在工业生产过程中会产生不同浓度的含铜废水,若没有得到有效的处理而进入环境,将会通过食物链对人们的身体健康产生极大危害.目前,工业上处理含铜废水的方法主要有化学混凝沉淀法、离子交换法和反渗透法等,但其所需成本较高,操作复杂,不宜大规模使用,而生物质材料吸附法去除水中重金属具有高效快速,成本较低,材料来源广泛等优点,近年来成为重金属净化处理研究的热点.
广西速生桉树资源丰富,其面积和产量都居全国首位,在桉树的开发和利用过程中会产生较多的树枝、锯末等废弃物.本文以桉树废弃物为植物模板,羟基磷灰石为修饰材料,通过遗态转化工艺制备出的新型桉树遗态HAP/C复合材料(PBGC-HAP/C),以此为吸附剂,探索其对含铜废水的吸附行为及其机制特征,以期为桉树高效利用及含铜废水的处理提供技术参考.
1 材料与方法 1.1 实验主要试剂及仪器
主要试剂: Ca (OH)2、(NH4)2HPO4、NaOH、HCl和HNO3等均为优级纯,Cu (NO3)2、氨水为分析纯,实验用水为超纯水.
主要仪器:原子吸收光谱仪(PE-AAnalyst700,美国)、水浴恒温振荡器(SHZ-B,上海)、X射线衍射仪(X'Pert PRO,荷兰)、傅里叶变换红外光谱仪(470 FTIR,美国)、马弗炉(SX2-5-12,上海) 等.
1.2 吸附剂制备
桉树废弃物经清洗干燥、抽提、烘干、焙烧、饱和氢氧化钙中浸泡、循环浸泡等工序获取吸附剂PBGC-HAP/C,具体制备方法: ①首先将原始木材切割为约30 mm×5 mm×5 mm尺寸的块体,然后在5%稀氨水中于100℃水浴条件下煮6 h,以进行抽提预处理,随后用超纯水洗净,并于80℃条件下干燥24 h. ②干燥后置于马弗炉中以400℃焙烧4 h. ③焙烧处理后样品在饱和氢氧化钙中浸泡48 h,然后在饱和氢氧化钙和0.02 mol·L-1磷酸氢二铵溶液中循环浸泡5次,每次2 h,最后在60℃条件下干燥24 h后获得成品. ④成品磨碎,过筛,即获得不同粒径的桉树遗态HAP/C复合材料(PBGC-HAP/C) 吸附剂.
1.3 实验方法
吸附实验:配置不同浓度的含铜模拟废水,用NaOH或HNO3调节pH值到相应指定值,然后取50 mL加入到100 mL的聚乙烯离心管中,且每个离心管中均投加0.5 g的PBGC-HAP/C吸附剂,在恒温水浴锅中振荡24 h,振荡频率150 r·min-1,将样品取出过0.22 μm滤膜,用火焰原子吸收分光光度法测定残余的Cu (Ⅱ) 浓度.
材料表征:采用SEM、EDS、XRD和FTIR分别对吸附前后PBGC-HAP/C吸附剂进行对比表征分析.
2 结果与讨论 2.1 溶液初始pH值对吸附的影响
将50 mL初始浓度分别为10、20、50 mg·L-1的Cu (Ⅱ) 溶液加入到100 mL的聚乙烯离心管中,pH值分别调为1~6.每个离心管中各加入0.5 g粒径小于100目的吸附剂,加盖密封,在25℃、150 r·min-1下恒温振荡24 h后过滤取样,分别测定水样Cu (Ⅱ) 浓度.
溶液体系的pH是影响吸附剂吸附性能的主要因素之一.在不同pH值条件下,PBGC-HAP/C吸附效果如图 1所示.结果显示pH=1时,吸附剂对Cu (Ⅱ) 基本没有去除效果,随着pH的增大,PBGC-HAP/C吸附性能呈现增大趋势,特别当pH>3后,10 mg·L-1、20mg·L-1的废水去除率保持在较高水平,达99%以上.这种现象主要是由于溶液体系pH不仅影响了吸附剂表面电荷的性状、离子化程度及种类,还控制了Cu (Ⅱ) 在溶液中的存在形态,从而导致吸附剂在强酸与弱酸条件下吸附性能存在较大差别.具体来看,吸附剂上附着有羟基磷灰石,溶液中存在式(1)、式(2) 化学平衡,当在pH<3强酸条件下,≡P-O-和≡Ca-OH基团消耗H+,两化学平衡向右进行,此时吸附剂表面的羟基磷灰石表面的基团主要以≡P-OH和≡Ca-OH2+形式存在,从而使吸附剂表面带正电,与H+产生竞争吸附.随着pH的升高,化学平衡向右移动的趋势减弱,此时吸附剂以吸附Cu (Ⅱ) 为主.有研究表明,当pH < 4时,Cu2+为主要存在形态;当pH在4~5之间时,主要形态为Cu (OH)+和Cu2+;当pH在5~6之间时,主要以Cu (OH)+,Cu (OH)2为主;当pH>6时,以Cu (OH)2沉淀为主.考虑到pH>5会改变复合材料的吸附机制特征,所以PBGC-HAP/C吸附剂对Cu (Ⅱ) 吸附的最佳pH值为5,后续实验pH值均为此值.
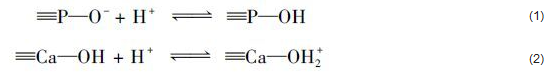
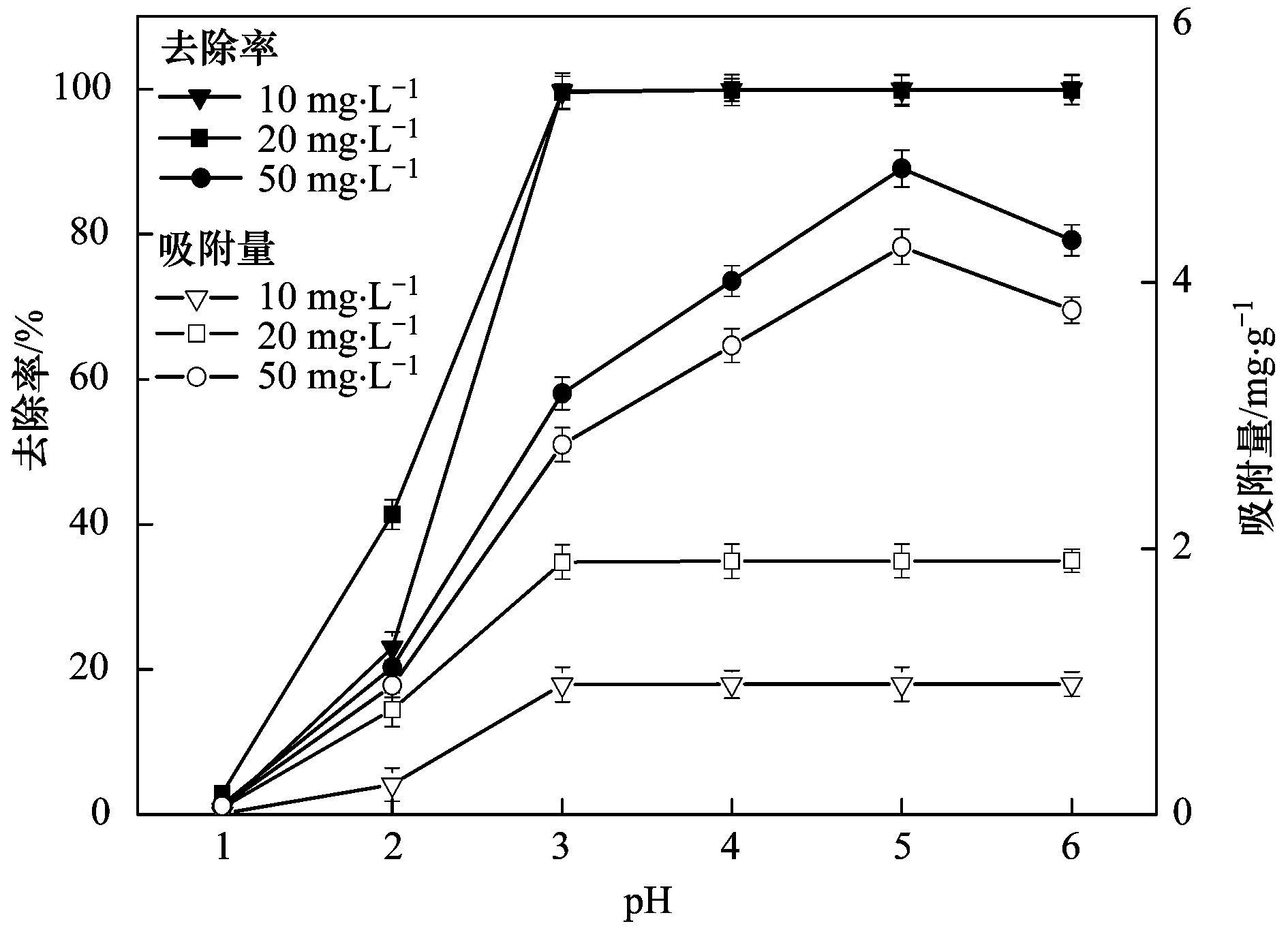
图 1 pH对PBGC-HAP/C吸附Cu (Ⅱ) 的影响
2.2 初始浓度对吸附效果的影响
将50 mL初始浓度分别为5~150 mg·L-1的Cu (Ⅱ) 溶液加入到100 mL的聚乙烯离心管中,pH值调为5.每个离心管中各加入0.5 g粒径小于100目的吸附剂,加盖密封,在25℃、150 r·min-1下恒温振荡24 h后过滤取样,分别测定水样Cu (Ⅱ) 浓度.
由图 2可见,当温度在25℃至45℃之间时,随着Cu (Ⅱ) 初始浓度的升高,PBGC-HAP/C吸附剂对Cu (Ⅱ) 的吸附量逐渐增加,吸附率在Cu (Ⅱ) 初始浓度达到30 mg·L-1之前基本保持稳定,而后才逐渐降低.由此说明初始浓度大于30 mg·L-1后,影响吸附效果的主要因素才是浓度,这可能是由于吸附剂一定量的情况下,金属离子浓度增大时,在复合材料活性点周围聚集更多的金属离子,从而吸附容量增加.浓度超过一定范围时,表面位点被充分占满,吸附剂已不能再吸附多余的重金属离子,吸附量接近饱和,去除率也就随之降低.从图 2中还可得知温度变化对复合材料对Cu (Ⅱ) 的吸附影响较大,特别当温度为45℃,Cu (Ⅱ) 浓度为150 mg·L-1时达到最大吸附量9.57 mg·g-1,可能是因为温度的升高使得吸附剂表面活化,使可利用的活性位点增多或者使吸附质的扩散速率增高,从而表现出升温有利于吸附.
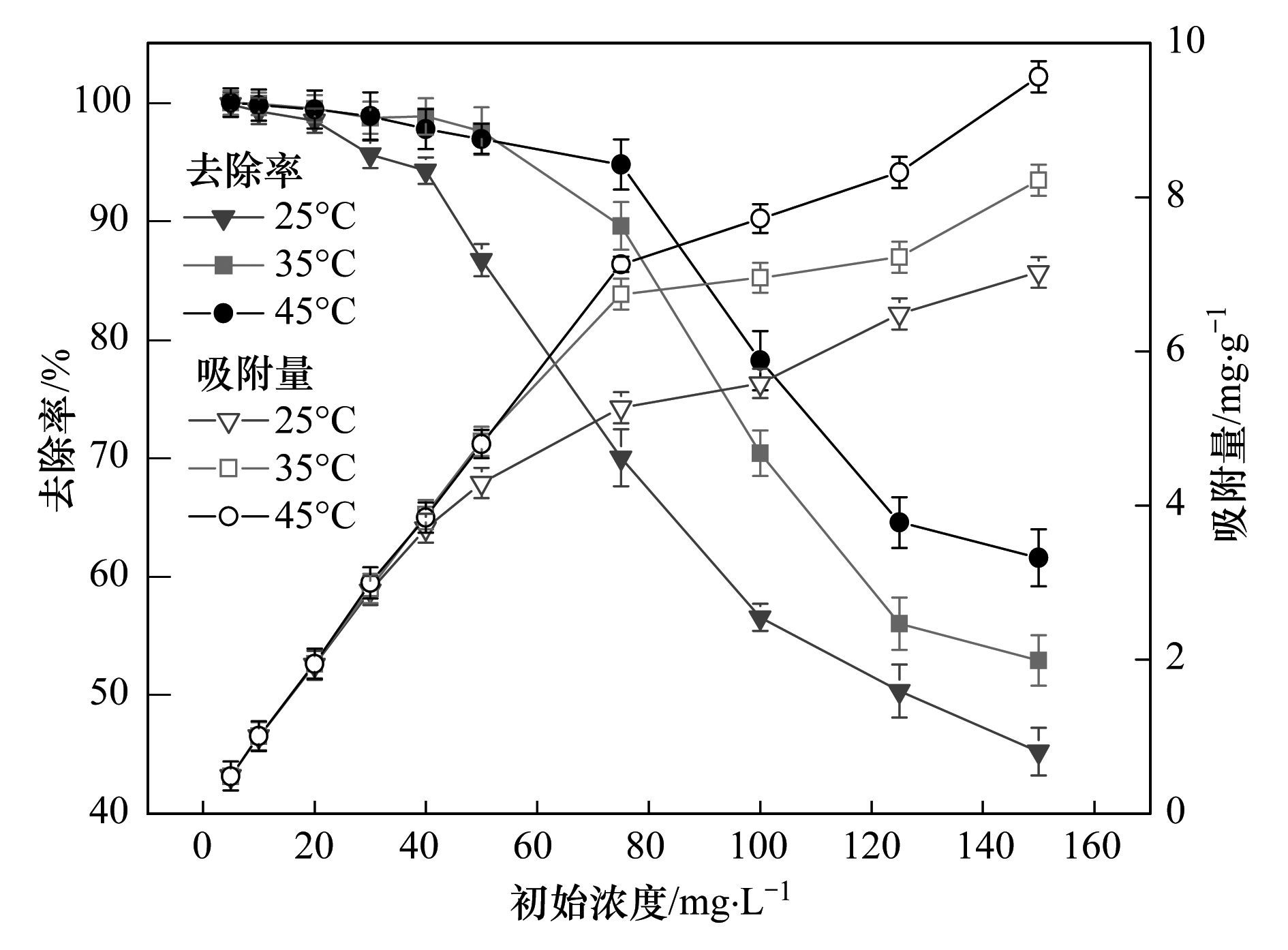
图 2 初始浓度对PBGC-HAP/C吸附Cu (Ⅱ) 的影响
2.3 吸附剂粒径对吸附效果的影响
将50 mL初始浓度分别为10、20、50 mg·L-1的Cu (Ⅱ) 溶液加入到100 mL的聚乙烯离心管中,pH值调为5.每个离心管中各加入不同粒径目数的吸附剂,加盖密封,在25℃、150 r·min-1下恒温振荡24 h后过滤取样,分别测定水样Cu (Ⅱ) 浓度.
从图 3可以看出,初始浓度为10mg·L-1时,吸附剂粒径对Cu (Ⅱ) 溶液的去除率无明显影响,对初始浓度为20 mg·L-1、50 mg·L-1的Cu (Ⅱ) 溶液吸附率影响较为显著.随着吸附剂粒径的减小,10、20和50 mg·L-1 Cu (Ⅱ) 的吸附率分别由97.29%、80.14%和75.29%增加到99.98%、99.59%和92.29%;吸附量由0.96、1.57和3.71 mg·g-1上升到0.98、1.95和4.55 mg·g-1. 表 1为不同粒径PBGC-HAP/C的比表面积,可以看出比表面与粒径大小没有明显的线性关系,根据图 4得知复合材料自身呈现固有的分级多孔结构,主要以介孔和微孔为主.因此,适当的研磨可以增大比表面积,但是过度的减小粒径使得吸附剂孔径结构被破坏或堵塞,造成比表面积呈现无规律变化,由此可以推断减小吸附剂粒径,影响吸附剂性能的主要因子不是比表面积.吸附剂粒径越小,Cu (Ⅱ) 的吸附率和吸附容量呈现增大的趋势,这可能有两种原因: ①从分子运动角度来看,相同质量的吸附剂经研磨、碎化、过筛等方式减小粒径,增强了吸附剂在液相中的布朗运动强烈程度,使铜离子与吸附剂接触几率加大,更易被吸附剂所吸附;②粒径较小的粉末状吸附剂,在液体中由于振荡作用较为松散,其固液接触面形成的膜容易更新,更易吸附溶液中的铜离子,而粒径较大块状的吸附剂,其比表面积虽与粉末状相差不大,但是块状材料中的分级多孔部分,其固液接触面形成的膜相对更新慢,从而引起吸附效果较粉末状稍差.在研磨碎化过程不会改变吸附剂表面化学性质,由此也可推断吸附过程存在物理吸附.因此实验过程中选取小于100目为适宜吸附剂粒径.同时还对材料改性前后做了对比,结果发现对含铜废水的处理效果优劣次序为HAP≥PBGC-HAP/C>炭化桉树粉末,PBGC-HAP/C的吸附效果与HAP相当,但其成本较低,具有潜在的使用价值.
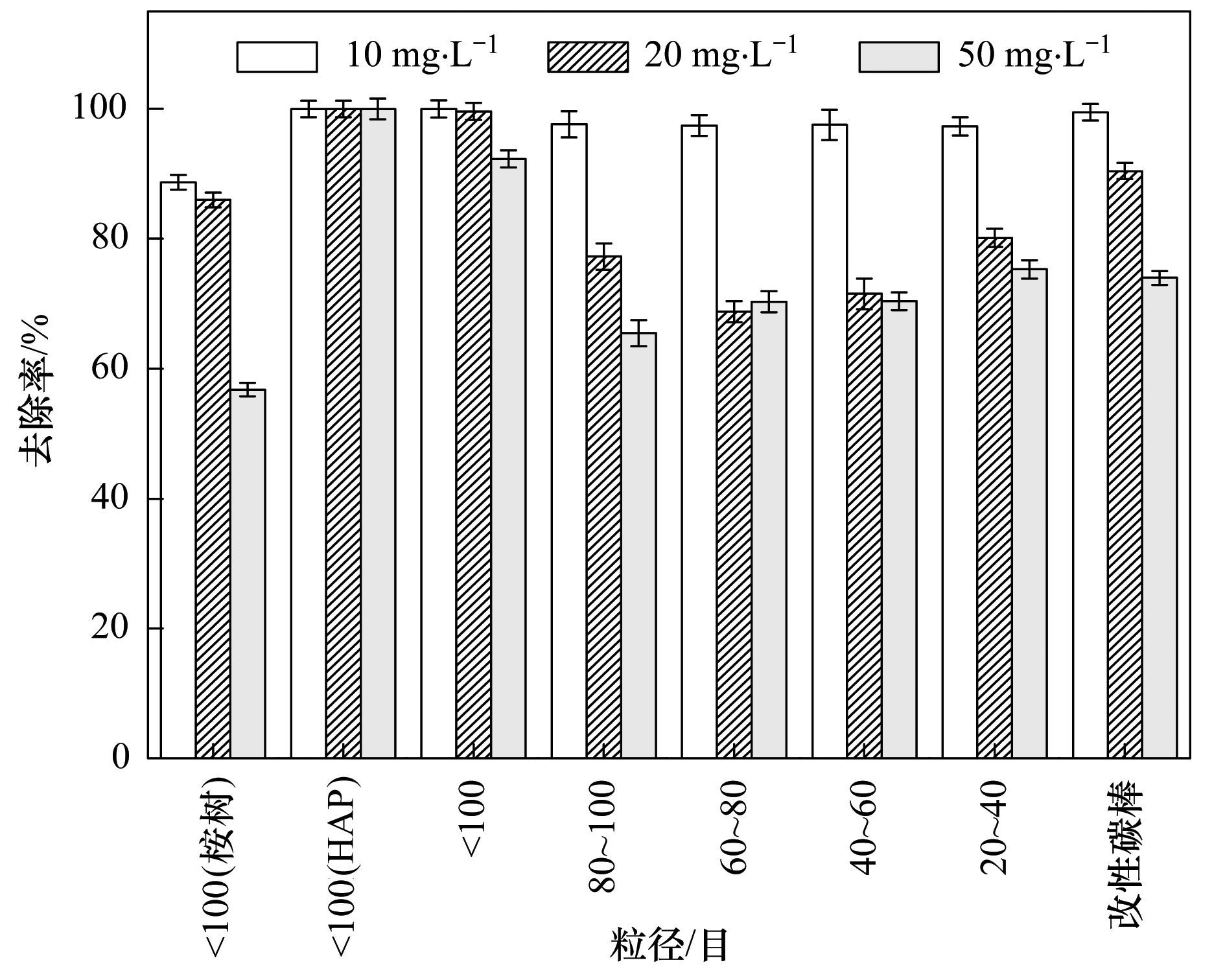
图 3 粒径对PBGC-HAP/C吸附Cu (Ⅱ) 的影响

表 1 不同粒径PBGC-HAP/C的比表面积
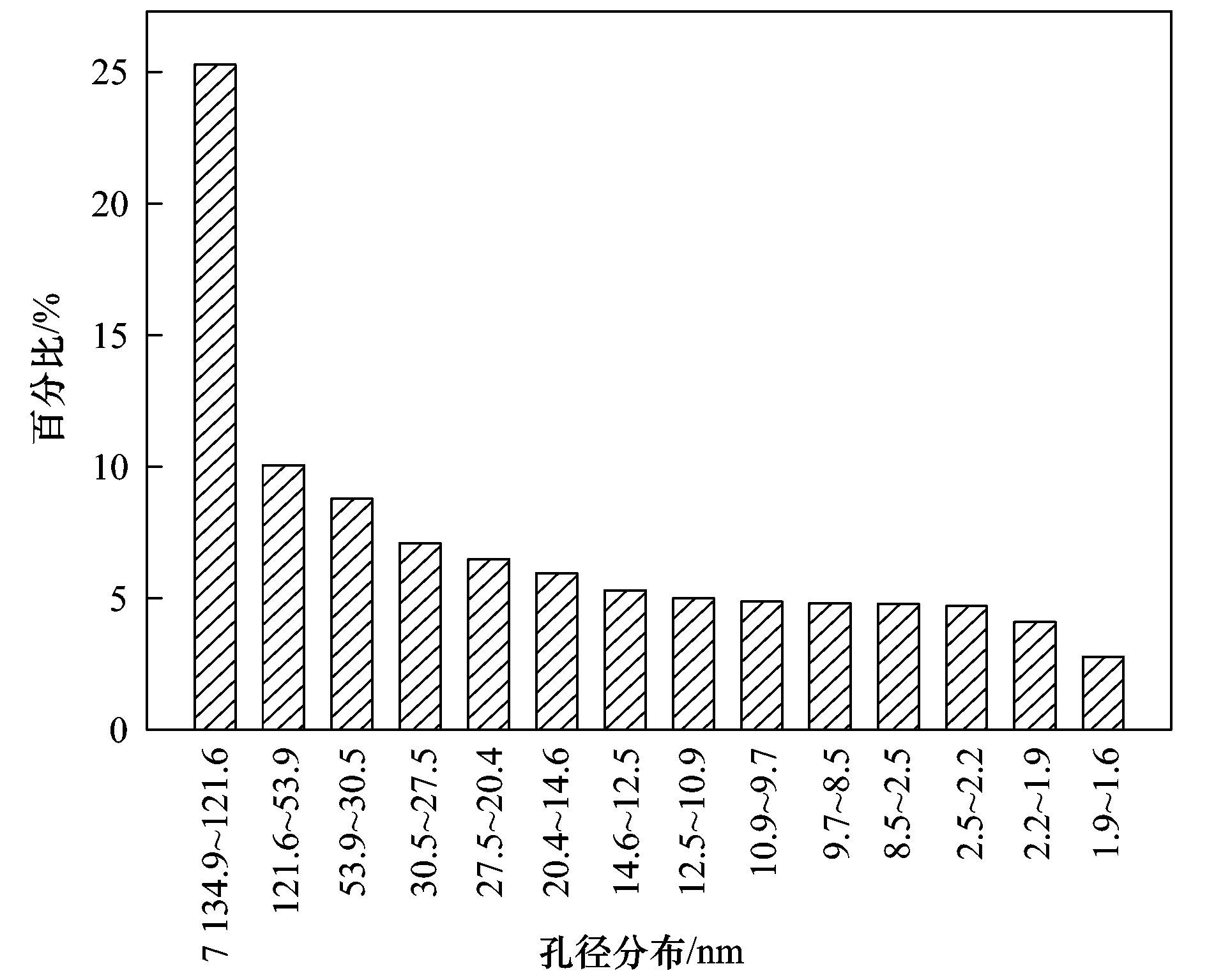
图 4 PBGC-HAP/C的孔径分布
3 HAP/C复合材料对水中Cu (Ⅱ) 的吸附机制分析 3.1 吸附动力学模型
在初始浓度分别为10、20、50mg·L-1,投加量为0.5g,pH值为5条件下,分析PBGC-HAP/C对水体中Cu (Ⅱ) 吸附动力学特征. PBGC-HAP/C对水体中Cu (Ⅱ) 的吸附量随时间的变化如图 5所示.从中可看出,在吸附的初始阶段,Cu (Ⅱ) 的吸附量随吸附时间的增加而快速上升,随后吸附速率逐渐减小,最后吸附量逐渐保持不变而达到平衡.在Cu (Ⅱ) 初始浓度为10、20、50 mg·L-1条件下,吸附容量随时间的变化分别在30、60、1 080 min后逐渐趋于平衡,与初始浓度为10 mg·L-1、20 mg·L-1相比,50mg·L-1的溶液则需要更长时间才能达到吸附平衡.在吸附初始阶段,吸附过程是以膜扩散为主的快速物理吸附,吸附剂表面存在大量可利用的吸附点位,加之吸附点位活性较高,从而使得吸附速率较快,随着吸附进行,吸附点位数量的减少及其活性降低,故反应速率也随之降低.
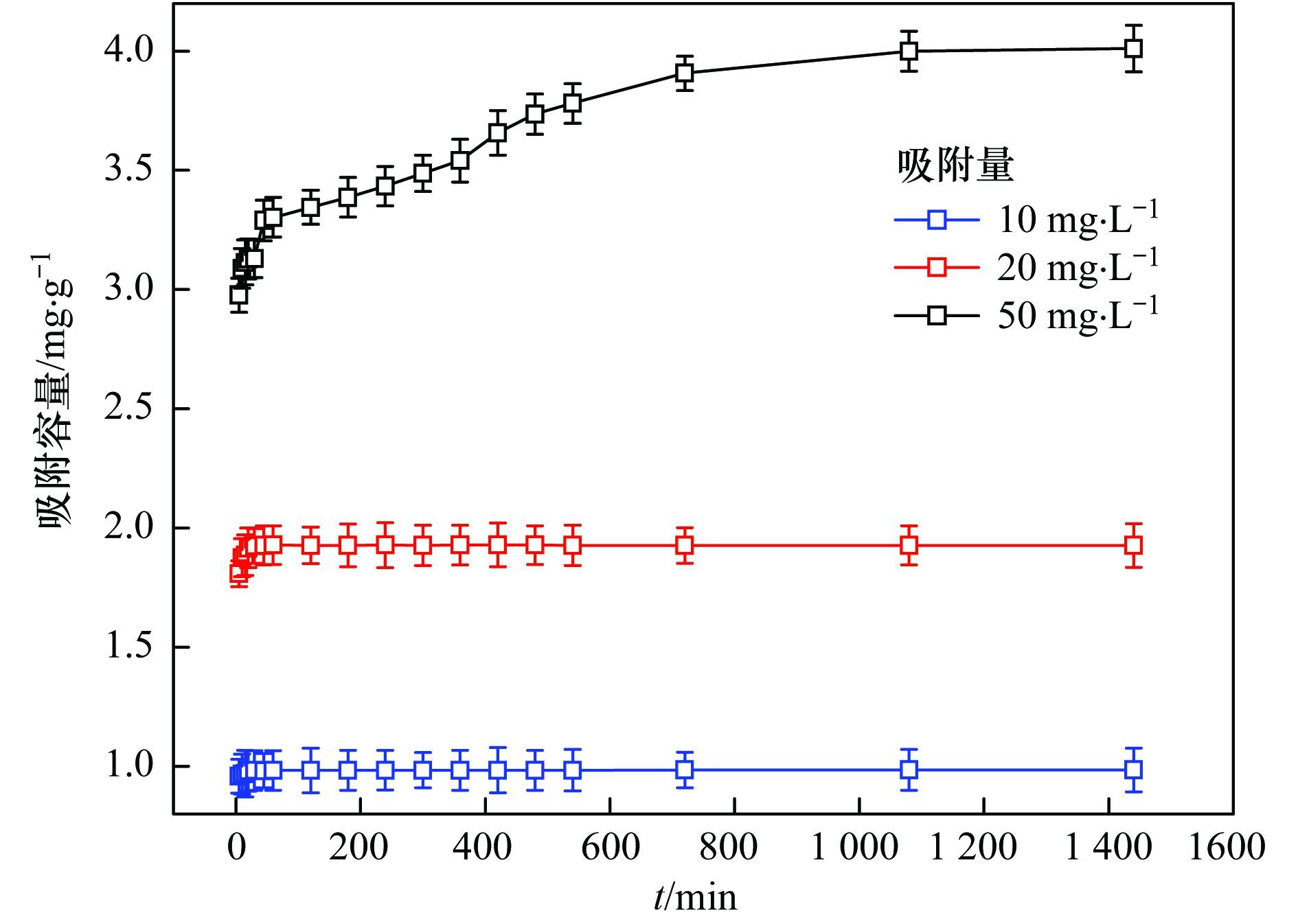
图 5 吸附容量随时间的变化
研究吸附动力学特征,分别应用了准一级、准二级方程的相关拟合计算,动力学方程式如下:
式中,qe和qt分别为平衡时和t时刻的吸附量,mg·g-1;k1为准一级动力学速率常数,min-1;k2为准二级动力学速率常数,g·(mg·min)-1;h为初始吸附速率,mg·(g·min)-1.
不同的动力学拟合参数如表 2所示.结果表明准二级动力学拟合所得到的吸附容量0.99、1.93、4.03mg·g-1和实验测得值0.99、1.93、4.05mg·g-1高度接近,其R2≥0.998,而准一级动力学方程算出的结果与实验测得值相差太大,说明准一级动力学存在局限性,准二级动力学模型能更加准确地描述PBGC-HAP/C对Cu (Ⅱ) 吸附动力学机制.化学键的形成是影响准二级动力学吸附作用的主要因子,由此也可推断该吸附过程以化学吸附为主[26].准二级动力学速率常数k2和初始吸附速率h随初始浓度的升高而降低,这可能是由于在吸附的初始阶段,过高的Cu (Ⅱ) 浓度,使得吸附过程中出现吸附点位临时“拥堵”现象,致使Cu (Ⅱ) 在吸附剂表面初始吸附速率较慢.
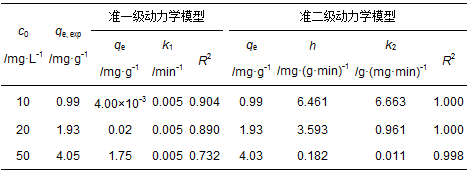
表 2 PBGC-HAP/C吸附动力学模型参数
3.2 等温吸附与热力学特征分析
本文采用Langmuir、Freundlich等温吸附模型对PBGC-HAP/C的吸附行为进行描述.各项参数可根据以下方程计算[27].
式中,qe、qmax分别为平衡吸附容量和理论最大吸附容量,mg·g-1;ce为平衡浓度,mg·L-1;b为吸附系数,L·mg-1;KF和n为Freundlich常数.
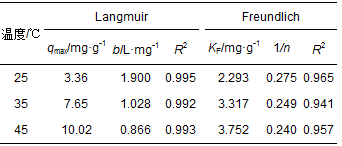
结果如表 3所示.可以得出,吸附剂对铜离子的吸附更加符合Langmuir吸附等温式,其相关性系数R2>0.99,高于Freundlich方程相关性,同时也表明吸附剂表面是比较均匀的,各处的吸附能力大致相同,其吸附属于单分子层吸附. Freundlich吸附模型中,一般认为0. 1 < 1 /n < 0. 5吸附容易进行,1/n>2吸附难以进行[28].从拟合结果可以得出吸附剂在不同温度下对铜离子的吸附均易进行,对吸附常数KF,KF,-45℃>KF,-35℃>KF,-25℃,表明升高温度有利于吸附,这与实验结果是相一致的.
表 3 PBGC-HAP/C等温吸附模型参数
无量纲化分离因子RL,其方程为RL=1/(1+bc0),它的大小能够用来表示吸附的性质,当0

图 6 不同温度下Cu (Ⅱ) 浓度对RL的影响
为了进一步探究温度变化对PBGC-HAP/C的吸附影响,本文通过计算吉布斯自由能(ΔGθ)、吸附焓(ΔHθ)、吸附熵(ΔSθ) 来确定吸附反应热力学效应,相应计算式如下:
式中,T为绝对温度,K;b为Langmuir吸附常数,L·mol-1;R为气体常数,8.314 J·(mol·K)-1.吸附焓和吸附熵可根据lnb和1/T的线性关系求出,相关参数如表 4所示.
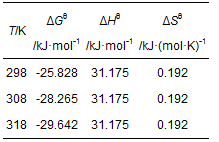
表 4 吸附热力学参数
吉布斯自由能为负值,说明该吸附过程为自发进行的,且随着温度增加,自发程度加大.在吸附过程中吸附焓和吸附熵分别为31.175 kJ·mol-1、0.192 kJ·(mol·K)-1,正的吸附焓表明吸附为吸热过程,升温有利反应进行.正的吸附熵ΔSθ表明在吸附过程中混乱度增加,这应该是较多的水分子在固/液界面发生吸附所致.
3.3 吸附材料表征分析 3.3.1 SEM/EDS分析
采用电子显微镜-能谱仪对材料吸附Cu (Ⅱ) 前后进行了扫描(如图 7).吸附前后SEM表征显示,吸附Cu (Ⅱ) 后没有出现明显的皱缩痕迹、形态畸变及结构坍塌现象,保留了对应植物模板天然的多孔结构,说明在吸附过程中PBGC-HAP/C复合材料能够抵挡水流冲刷负荷,拥有稳定的遗态结构. EDS分析显示,在吸附前的材料上检测出了大量的C、O、Ca、P元素和少量的原始桉树木材含有的Al元素,其中Ca/P质量比值约为2.49,与羟基磷灰石[Ca5(PO4)3(OH)]中的Ca/P质量比值2.15接近,这表明羟基磷灰石成功附着在桉树遗态结构上.在吸附后材料上检测出了Cu元素,结合SEM扫描结果,所制备的材料呈现出不同规则的多孔空隙,且表面负载了羟基磷灰石,由此可得出铜元素主要吸附在材料孔隙且具有羟基磷灰石的周围.同时根据测试,材料主要由碳和羟基磷灰石组成,其中羟基磷灰石占复合材料的质量分数为4.27%,因此可推断PBGC-HAP/C吸附Cu (Ⅱ) 是由于碳和羟基磷灰石共同作用,其主要途径为吸附作用.

图 7 PBGC-HAP/C吸附Cu (Ⅱ) 前后的SEM/EDS图
3.3.2 XRD分析
对吸附后的材料的X射衍射图进行分析(如图 8).从图 8中可知PBGC-HAP/C无明显的晶体结构,表明其为无定形,吸附前材料在2θ为25.80°、31.87°、39.57°、72.66°和88.26°等平面上的衍射峰为HAP的特征,再次证明在桉树遗态结构上已成功合成了HAP[32].吸附后其主峰未见明显偏移,但峰的强度出现明显增强,这表明是钙羟基磷灰石与铜发生化学反应,部分目标元素Cu替代了PBGC-HAP/C中的Ca元素位置,吸附过程中生成了新的物质.
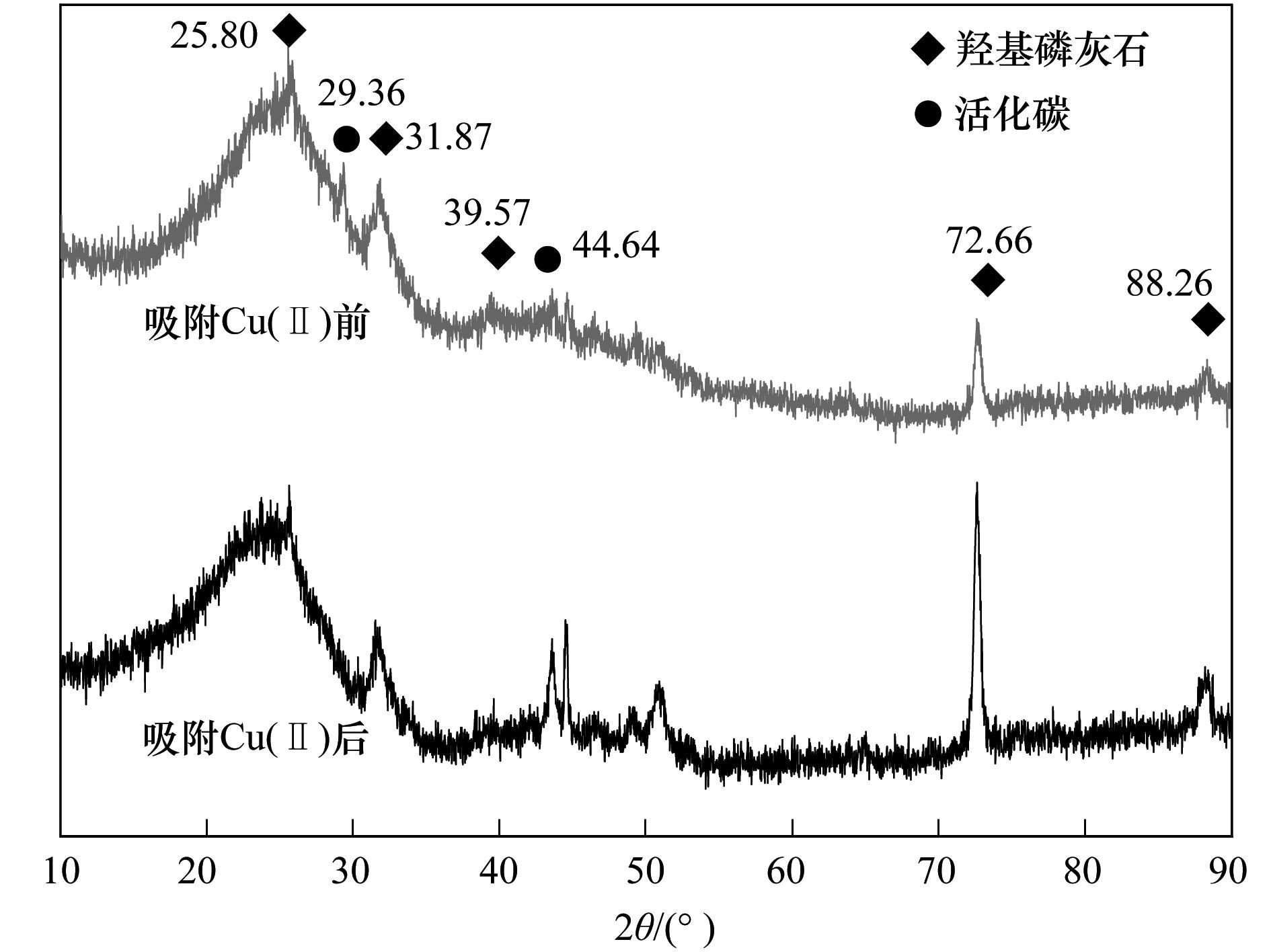
图 8 PBGC-HAP/C吸附Cu (Ⅱ) 前后的XRD图
3.3.3 FTIR分析
对吸附后的材料进行FTIR分析,结果如图 9所示. 3 449.06、1 575.56和1 287.73 cm-1处的峰分别偏移减弱,Cu (Ⅱ) 吸附在O-H、CO基团上影响了基团伸缩振动位置,表明在吸附过程中发生了化学反应;1 050.53 cm-1处的H2PO4-、PO43-的吸收峰减弱,说明磷灰石的结构发生了改变,H2PO4-、PO43-参与了吸附过程,878.28 cm-1处新出现的应为C-C键,表明吸附过程有旧含氧和含碳主要特征官能团的化学键断裂和新的化学键生成.由此表明吸附剂表面的官能团在一定程度上决定了其吸附的性质,改性后的吸附剂表面官能团数量增加,在一定程度上可以提高了其吸附能力.
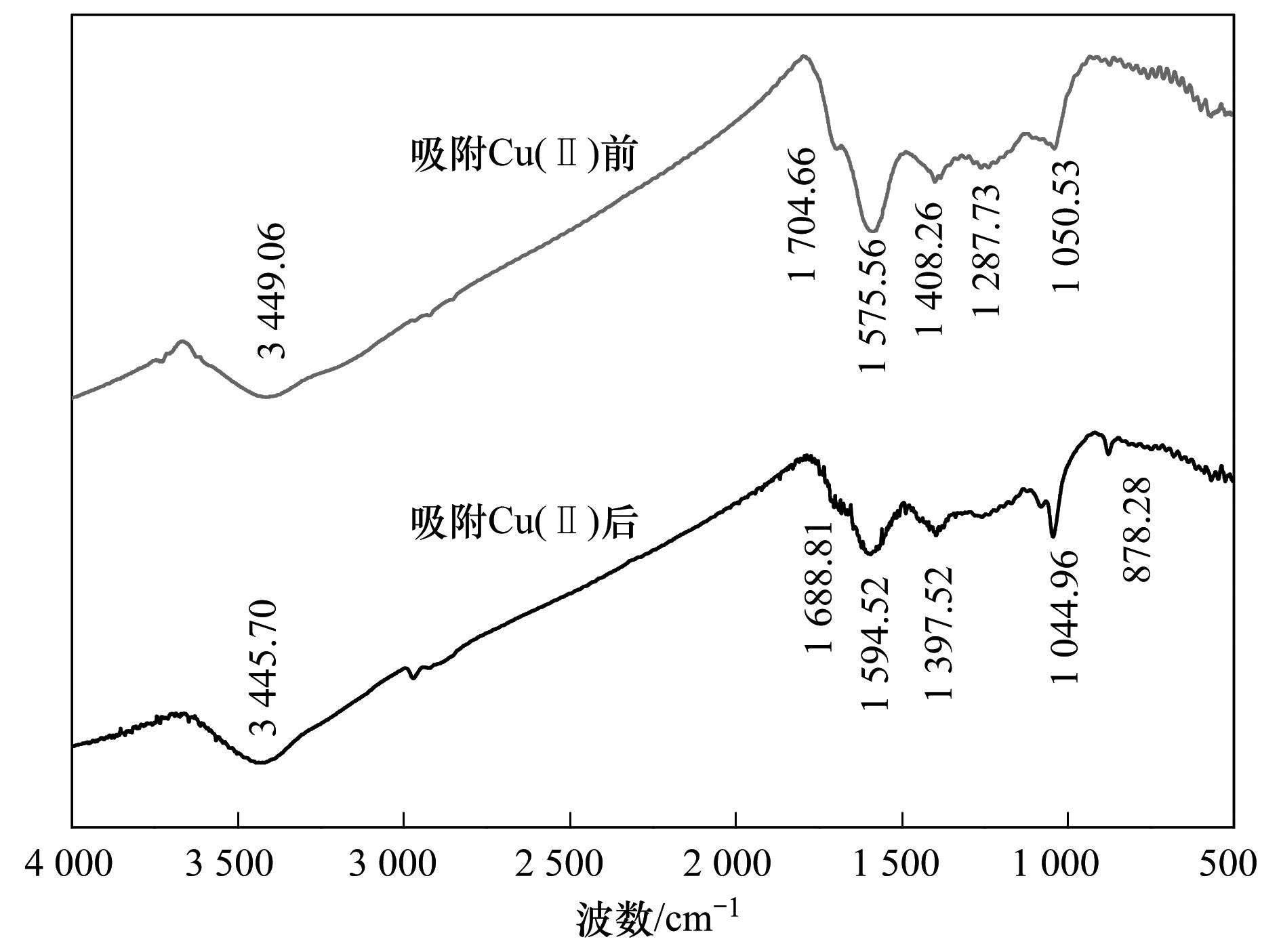
图 9 PBGC-HAP/C吸附Cu (Ⅱ) 前后的FTIR图
3.4 吸附机制特征分析
通过以上分析得知PBGC-HAP/C的吸附Cu (Ⅱ) 主要是以化学吸附为主,而吸附体系不同的pH值会影响吸附的机制.在溶液体系pH<3时,溶液体系中H+浓度较大,PBGC-HAP/C吸附剂上的官能团易与带正电的氢离子结合而被质子化带正电,同时铜离子又是溶液主要的离子形态,从而可能会与铜离子发生静电排斥,使铜离子的吸附处于劣势.有研究表明在溶液中pH<1时HAP完全溶解,HAP对溶液的金属离子固定明显降低,所以才导致当pH=1时吸附剂对铜去除效果不明显.当pH值在较低范围时,吸附作用对铜离子浓度降低影响甚微,主要原因是HAP在pH较低时溶解产生大量的PO43-,重金属离子和PO43-作用形成磷酸盐沉淀,这与FTIR表征结果是相一致的.随着pH升高后,吸附剂质子化程度逐渐减小,H+吸附竞争力下降,此时溶液主要以吸附铜离子为主,带负电的PBGC-HAP/C与带正电的Cu (Ⅱ) 发生静电吸引,致使吸附剂与铜发生了离子交换与表面络合作用.因此本文归纳了吸附过程中可能存在机制(如图 10): ①物理作用. HAP/C复合材料依靠比表面积和孔隙结构特点,为Cu (Ⅱ) 提供吸附点位,正如2.3节中所述通过研磨碎化减小吸附剂的粒径可以提高吸附效果. ②化学络合作用.桉树碳为纤维素、木质素、半纤维素等天然聚合物交联聚合而成,因此含有大量的羟基,加之负载羟基磷灰石,所以新型的HAP/C复合材料具有大量的含氧官能团(主要为O-H),O有孤对电子,而Cu (Ⅱ) 提供空轨道,所以吸附剂与Cu (Ⅱ) 发生表面络合作用[式(9)、式(10) ],这在整个吸附过程中起到最重要的作用. ③静电作用.吸附体系的pH值影响吸附剂表面的电性.在弱酸条件下,吸附剂表面带负电,即Cu (Ⅱ) 与复合材料结构负电荷位(HAP/C-) 和表面荷负电基团(-O-基团) 产生静电吸附作用[式(11)、式(12) ]. ④离子交换作用.在酸性溶液中羟基磷灰石存在溶解平衡[式(13) ],生成的Ca (Ⅱ) 可与Cu (Ⅱ) 发生等电荷离子交换[式(14) ],使溶液的铜离子减少,同时也印证了H2PO4-参与了吸附过程.

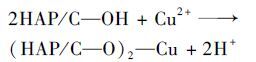





图 10 吸附机制示意
3.5 PBGC-HAP/C与其他吸附剂的比较
PBGC-HAP/C对Cu (Ⅱ) 的吸附情况与近年来报道的其他同类吸附剂材料做对比(如表 5),可以看出溶液pH为5时,PBGC-HAP/C的吸附能力要好于其中大部分改性吸附剂,稍逊于微波辅助NaOH改性的竹炭,但是相对PBGC-HAP/C复合材料而言,其桉树原材料来源丰富、成本较低、制备工艺简单且拥有稳定的遗态结构,可以成为一种很好的吸附材料.此外,吸附剂对Cu (Ⅱ) 的吸附大部分都符合Langmuir等温吸附模型,但是它们的主要吸附机制却不一致,由前面分析可知PBGC-HAP/C对Cu (Ⅱ) 吸附机制主要为化学络合作用.具体参见污水宝商城资料或http://www.dowater.com更多相关技术文档。
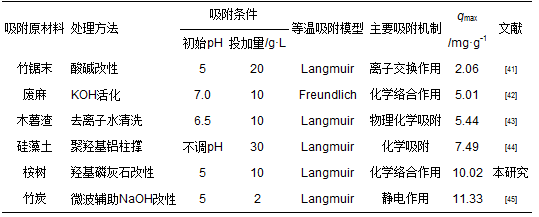
表 5 不同吸附材料对Cu (Ⅱ) 的吸附能力
4 结论
(1) 初始溶液体系pH和浓度对PBGC-HAP/C吸附Cu (Ⅱ) 的性能影响较大.当pH=5左右,吸附效果最佳,升高浓度吸附效率呈下降趋势;通过研磨碎化减小粒径,可以提高吸附剂吸附性能.
(2) 吸附初始阶段,吸附速率较快,随时间延长吸附量逐渐趋于平衡,与初始浓度为10 mg·L-1、20mg·L-1相比,50mg·L-1的初始浓度需要更长时间才能达到吸附平衡,通过动力学模型拟合,准二级动力学更能准确地描述吸附过程,其相关性系数R2均大于0.998,表明吸附过程主要是以化学吸附为主.
(3) 根据吸附热力学计算,ΔGθ为负值,ΔSθ和ΔHθ都为正值,表明PBGC-HAP/C吸附Cu (Ⅱ) 是一个自发、墒增的吸热过程,温度升高有利于吸附的进行. Langmuir等温模型更符合其吸附过程,表明该过程主要是单分子层吸附.
(4) PBGC-HAP/C对Cu (Ⅱ) 吸附机制存在多种情况,包括物理吸附、化学吸附、静电吸附、离子交换作用,但其主要的机制为PBGC-HAP/C表面大量的含氧官能团与Cu (Ⅱ) 发生化学络合反应使得Cu (Ⅱ) 被去除,且此反应伴随整个吸附过程.